11月29日,亚宝药业发布公告称,公司收到了国家药监局核准签发的苯甲酸阿格列汀片《药品注册批件》。数据显示,苯甲酸阿格列汀片最早由日本武田药品工业株式会社研发,于2010年在日本上市,2013年在中国获批进口药品上市,商品名“尼欣那”。
表1:药品注册批件主要内容
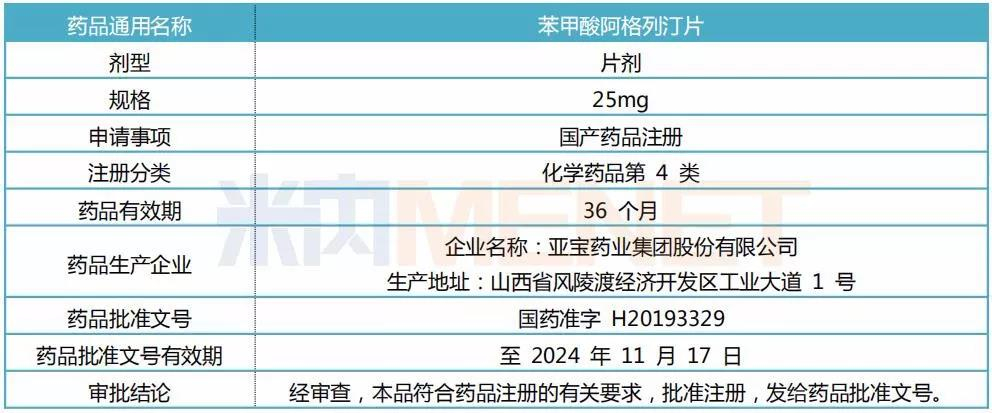
(来源:公司公告)
图1:中国公立医疗机构终端化学药口服糖尿病用药年度销售趋势(单位:万元)
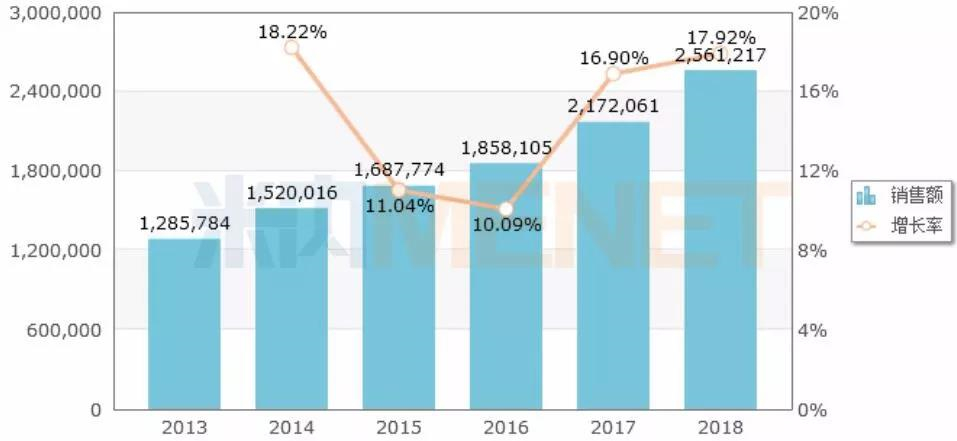
11月29日,亚宝药业发布公告称,公司收到了国家药监局核准签发的苯甲酸阿格列汀片《药品注册批件》。数据显示,苯甲酸阿格列汀片最早由日本武田药品工业株式会社研发,于2010年在日本上市,2013年在中国获批进口药品上市,商品名“尼欣那”。
表1:药品注册批件主要内容
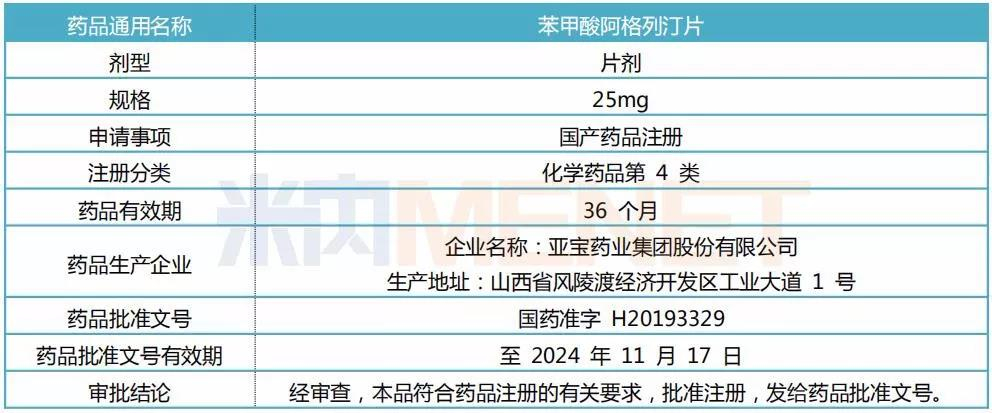
(来源:公司公告)
图1:中国公立医疗机构终端化学药口服糖尿病用药年度销售趋势(单位:万元)
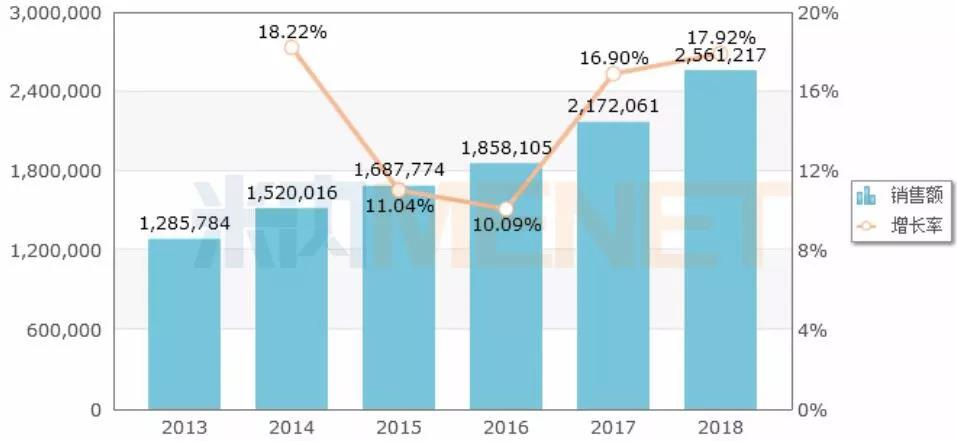
据悉,苯甲酸阿格列汀片主要适用于治疗2型糖尿病,最早由日本武田药品工业株式会社研发,于2010年在日本上市,米内网跨国上市公司销售数据库数据显示,2017年该产品的全球销售额为537亿日元(约为5亿美元)。
2013年,原研产品在中国获批进口上市,商品名“尼欣那”,2018年在中国公立医疗机构终端销售额达6285万元,增长率为187.68%,该产品为2019版国家医保目录乙类产品,产品进入国产化后将迎来市场放量。
亚宝药业在公告中提到,公司首次提交苯甲酸阿格列汀片注册申请的受理时间为2017年2月22日,目前除该公司外国内尚无其他公司取得苯甲酸阿格列汀片药品注册批件。截至目前,公司在该产品研发项目上已投入研发费用约为889万元人民币。
米内网MED中国药品审评数据库2.0数据显示,截至2019年11月29日,苯甲酸阿格列汀片在审的仿制上市申请企业还有深圳市海滨制药、石药欧意药业、湖南千金湘江药业、国药集团国瑞药业、广东东阳光药业、江苏诺泰澳赛诺生物制药、江苏中天药业、江苏德源药业,注册分类均为4类仿制。



